LATIHAN DAN KUIS 8
LATIHAN
Tetapan kesetimbangan reaksi H2 + I2 ⇌ 2HI adalah 50 pada 600 K, tentukan tetapan kesetimbangan untuk HI ⇌ ½ H2 + ½ I2
JAWABAN
Untuk reaksi: H2 + I2 ⇌ 2HI
➡ Kc =
Untuk reaksi: HI ⇌ ½ H2 + ½ I2
➡ K'c =
Perhatikan reaksi kesetimbangan berikut:
![]()
Apabila pada volume tetap pada temperatur dinaikkan, keserimbangan bergeser kearah…
a. Kanan dan harga K tetap
b. Kiri dan harga K kecil
c. Kanan dan harga K semakin besar
d. Kanan dan harga K semakin kecil
e. Kiri dan harga K makin besar
Pembahasan:
Kenaiakan temperatur menyebabkan kesetimbangan bergeser kekanan, kearah hasil dan harga K naik.
Jawaban : C
Suatu reaksi dapat balik dikatakan mencapai keadaan setimbang jika..
a. Harga tetapan kesetimbangan Kc = 1
b. Harga tetapan kesetimbangan Kc = 0
c. Kecepatan reaksi kekanan sama dengan kekiri
d. Jumlah mol zat sebelum dan sesudah reaksi sama
e. Massa zat sebelum dan sesudah reaksi sama
Pembahasan:
Mula-mula reaksi A dan B berkurang dengan cepat, kemudian tidak begitu cepat, dan akhirnya mencapai harga yang tetap. Keadaan sistem yang demikian disebut setimbang.
Jawaban : C
13. Diketahui reaksi :
2A(s) + B(l) → 3C(s) +2D(g)
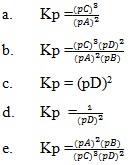
Pembahasan
Zat-zat pereaksi dipangkatkan koefisiennya akan mempunyai harga tetap. Jika reaksi itu dalam wujud solid dan liquid maka diabaikan.
Jawaban : C
Pada suhu tertentu dalam ruang tetutup yang bertekanan 10 atm terdapat dalam keadaan setimbang 0,3 mol gas SO2 ; 0,1 mol gas SO3 ; dan 0,1 mol gas O2 dengan reaksi :
![]()
Harga Kp pada suhu tersebut adalah…
a. 36 atm
b. 18 atm
c. 9 atm
d. 4,5 atm
e. 0,05 atm
Pembahasan:
Karena sudah dalam keadaan setimbang, dapat kita cari nt.
nt = 0,3 mol + 0,1 mol + 0,1 mol = 0,5mol
Pt = 10 atm
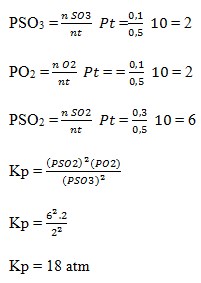
Jawaban : B
KUIS
Nilai tetapan kesetimbangan untuk reaksi N2 + 3H2 ⇌ 2NH3 adalah K, tetapan kesetimbangan untuk
JAWABAN
Untuk reaksi:
N2 + 3H2 ⇌ 2NH3
Kc = K =
Serupa dengan persamaan itu maka
K'c =
Jadi K'c2 = Kc = K → K’c =
Suatu sistem kesetimbangan bersifat dinamis-mikroskopis berarti…
a. Perubahan berlangsung terus-menerus dan dapat diamati
b. Reaksi terus berlangsung kekanan dan kekiri dan dapat diamati
c. Reaksi terus berlangsung kekanan dan kekiri tetapi tidak teramati
d. Perubahan berlangsung terus berhenti sehingga tidak dapat diukur
e. Perubahannya terhenti dan dapat terukur
Pembahasan :
Kesetimbangan dinamis yaitu proses bolak-balik dengan laju yang sama untuk kedua arah. Jadi reaksi berlangsung kekanan dan kekiri. Bersifat dinamis-mikroskopis maksunya hanya terjadi sedikit perubahan jadi tidak teramati.
Jawab
Berikut adalah faktor-faktor yang mempengaruhi kesetimbangan suatu reaksi reversible, kecuali…
a. Suhu
b. Volume
c. Tekanan
d. Konsentrasi
e. Katalisator
Pembahasan :
Faktor-faktor yang mempengaruhi kesetimbangan yaitu suhu, konsentrasi, tekanan, dan volume.
Jawaban : E


Tidak ada komentar:
Posting Komentar